消化在线: 炎症性肠病生物制剂治疗的药物监测进展
来源:
原文:
Advances in
Therapeutic Drug Monitoring of Biologic Therapies in Inflammatory Bowel
Disease: 2015 in Review.
Curr Treat Options
Gastroenterol. 2016 Feb 5.
解读:
主要观点
抗肿瘤坏死因子α单抗(抗TNF-α单抗)的出现对炎症性肠病治疗具有突破性意义。然而,有部分患者对该药物无效,或最初有效后来失效。早期的临床试验显示抗TNF-α单抗治疗无效和抗TNF-α单抗的血药浓度以及抗TNF-α单抗抗体(以下简称:抗抗体)的产生有关。最近的研究提供了更多的证据,支持抗TNF-α单抗治疗无效和其谷浓度低及抗抗体产生有关。通过药物监测,根据血药浓度及抗抗体产生的情况调整治疗,可以提高疗效。而且,对抗TNF-α单抗治疗有效的患者,仍需要进行预期的药物监测,以确保合适的给药剂量和不产生抗抗体。另外,对那些有抗抗体,但水平较低的患者,应增加抗TNF-α单抗的给药剂量或加用免疫抑制剂(有助于减少抗TNF-α单抗和其抗抗体的抗原抗体反应)。
概述
炎症性肠病(Inflammatory
bowel disease, IBD)是一组病因尚不十分清楚地慢性非特异性肠道炎症性疾病,包括克罗恩病(Crohn’s disease, CD)和溃疡性结肠炎(ulcerative colitis, UC)。直接针对IBD的炎症因子(肿瘤坏死因子)的单克隆抗体的出现,是IBD治疗药物的重大突破。英夫利西是FDA批准的第一个抗肿瘤坏死因子α单抗,最初用于CD的诱导和缓解,后来也批准用于UC的治疗。目前又有了一些新的抗肿瘤坏死因子α单抗,如阿达木单抗(一种人源的抗肿瘤坏死因子α单抗)、赛妥珠单抗、戈里木单抗等。英夫利西使很多IBD患者避免了肠切除手术,尤其是CD患者。然而,有部分患者对该药物无效,或最初有效后来失效。有研究显示抗TNF-α单抗治疗无效和抗TNF-α单抗的血药浓度以及抗TNF-α单抗抗体(以下简称:抗抗体)的产生有关。通过药物监测,可以提高治疗效果。本文对相关文献进行了综述。
抗TNF-α单抗血药浓度、抗抗体产生和治疗效果之间相互关系
目前的许多临床研究支持抗TNF-α单抗药物是否持续有效,与药物的血药浓度和抗抗体产生有关。抗TNF-α单抗的血药浓度和给药剂量呈线性相关,但各生物制剂的半衰期不同,英夫利西的平均半衰期是7.7-9.5天,阿达木的半衰期是英夫利西的两倍。
抗TNF-α单抗的血药浓度影响临床疗效。Maser等研究显示血药浓度水平越高,内镜评分和CRP水平越低。Baert等提出用药后第四周,英夫利西血药浓度应大于12ug/ml。Van等也发现CDAI和炎症指标与英夫利西的血药浓度有关。谷浓度水平>1.0ug/ml者在30周的缓解率更高(72.8%和58.2%),SUCCESS试验得到相似的结果。在UC患者,监测英夫利西血药浓度可提高粘膜愈合率(OR 7.3, 95%CI 2.9-18.4),不进行药物监测组的结肠切除手术率更高(OR 9.3, 95%CI 2.9-29.9)。有趣的是,在阿达木单抗和赛妥珠单抗早期的临床试验,这种影响不确定。然而,最近的研究,特别是阿达木单抗,显示有同样的趋势。关于戈里木单抗的研究显示血药浓度高的组,临床有效和缓解率也较高。
抗TNF-α单抗抗体的产生是血药浓度降低的重要原因之一。大部分研究支持产生了抗英夫利西抗体的患者,药物的有效率降低。然而,也有存在争议的结果,认为抗英夫利西抗体的产生不影响治疗效果。同样,阿达木单抗和赛妥珠单抗的初期研究结果也不一致。Karmiris等研究显示抗阿达木抗体产生和诱导、维持缓解无关。然而,一项小样本(40例)的日本人群的横断面研究显示产生抗阿达木抗体的患者的ESR和CRP更高,产生抗赛妥珠单抗抗体的患者26周缓解率降低。虽然存在争议,但目前大部分专家同意抗TNF-α单抗失效和抗抗体形成有关。
综上,使用抗TNF-α单抗药物时,进行药物监测有助于提高药物疗效,且回顾性研究显示治疗药物监测可降低总花费。对于抗TNF-α单抗治疗无效的患者,如果药物监测提示谷浓度低,则应增加给药剂量或缩短给药间隔;而如果血药浓度是足够的,抗抗体阴性,则应该改用其他药物。如果药物监测提示存在高水平的抗抗体,应考虑改用其他的抗TNF-α单抗;而如果抗抗体呈低水平,可考虑加用免疫抑制剂,如硫唑嘌呤或甲氨蝶呤,有可能使抗抗体减少或消失(见图1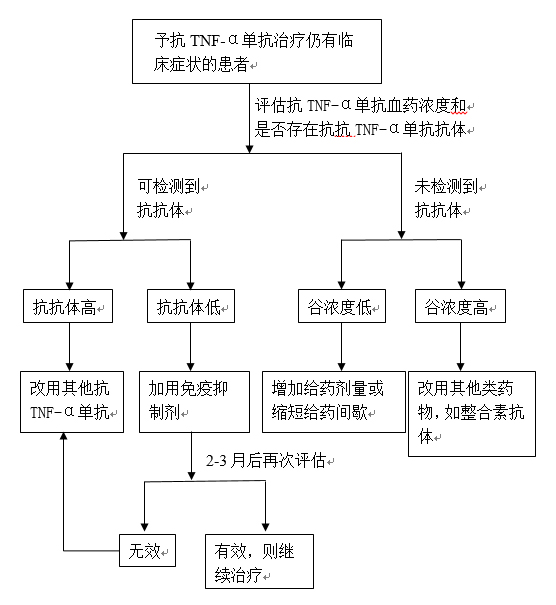
图1. 药物监测流程图
2015年生物制剂药物监测的研究进展
1. 英夫利西的血药浓度应达到3-8ug/ml,阿达木单抗的血药浓度应维持在7-12ug/ml
Ungar等的观察发现无论使用英夫利西还是阿达木单抗,血药浓度和粘膜愈合相关,粘膜愈合组的血药浓度是未达到粘膜愈合组的两倍以上。英夫利西血药浓度大于3ug/ml、阿达木单抗大于7.1ug/ml对达到内镜下粘膜愈合具有强烈的预测作用。但是英夫利西血药浓度大于8ug/ml、阿达木单抗大于12ug/ml,达平台期,将不再能提高粘膜愈合率。也就是说如使用英夫利西,血药浓度应达到3-8ug/ml;如使用阿达木单抗,血药浓度应维持在7-12ug/ml。
2. 血药浓度和病变局部的药物浓度可能不一致
通常认为血药浓度和肠道病变局部的抗TNF药物浓度是一致的。然而,Yarur等观察了15例活动期患者,11例的血药浓度远高于病变组织中的药物浓度,考虑可能是是继发于肠腔蛋白的丢失。有待更多研究。
3. 阿达木单抗的谷浓度大于4.5ug/ml仍无效的患者,继续增加药物剂量获益很小;但英夫利西谷浓度大于3.8ug/ml仍无效的患者,增加药物剂量仍有获益的可能。
Yanai等分析了247例英夫利西或阿达木单抗治疗无效的IBD患者(均进行了药物监测)的临床转归,发现阿达木单抗谷浓度大于4.5ug/ml,增加药物剂量仍无效的阳性预测值为85%,改用其他类药物治疗有效的阳性预测值为100%。即对于阿达木单抗的谷浓度大于4.5ug/ml仍无效的患者,继续增加药物剂量获益很小。有趣的是,英夫利西的结果不太相同,当谷浓度大于3.8ug/ml, 增加药物剂量仍无效的阳性预测值为65%,改用其他类药物治疗有效的阳性预测值为72%。该研究也检测了抗抗体,提示在低水平或无抗抗体组,增加药物剂量可提高有效率(p=0.001)。还观察到在低水平或无抗抗体组,增加给药剂量后血药浓度增加(p<0.001),而在高水平抗抗体组,增加给药剂量前后血药浓度无统计学差异。这个研究的结果支持在存在低水平抗抗体者,应增加给药剂量(以前的策略是加用免疫抑制剂,如硫唑嘌呤、甲氨蝶呤、6-巯基嘌呤等)。
4.Vande等根据谷浓度调整英夫利西治疗的研究(TAXIT)具有里程碑意义,是最早报道的药物监测有效的研究之一。明确提出通过药物监测调整治疗,可以降低临床复发率,减少维持治疗的费用。早期开始进行药物监测可以使英夫利西的临床应答最大化。
安全性
英夫利西和抗英夫利西抗体结合增加输液反应的风险,尤其当抗抗体大于8ug/ml。尚不明确增加给药剂量是否导致不良反应增加。目前两项大样本的回顾性试验显示血药浓度高未增加并发症的发生率。
小结
在生物制剂治疗IBD中,监测抗TNF-α单抗血药浓度和是否产生抗抗体有很大价值。不仅可以通过提高抗TNF-α单抗的药物疗效,而且可以使药效最大化。
网站声明:本网站刊载内容为内部交流使用,刊载内容仅代表作者个人观点与本网站无关,且不做为任何治疗依据和参考。因刊载内容影响读者相关利益本网站及作者均不负责。注明来源本网站的文字、图片、视频等资料,版权归网站所有,著作权归作者所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理,因作者导致的版权侵权由作者承担全部责任。所有活动最终解释权归医学顾问网所有。特此声明!